Być może mało kto o tym wie, ale Ministerstwo Zdrowia starannie pilnuje, aby system zgłaszania NOP był w Polsce jedną wielką fikcją, odrzucając wszelkie pomysły na usprawnienie zgłaszania niepożądanych odczynów poszczepiennych.
I zgodnie ze staraniami Ministerstwa Zdrowia w Polsce zgłaszanych jest najmniej NOP w całej Europie, czyli zaledwie 15 na 100tys. szczepień:
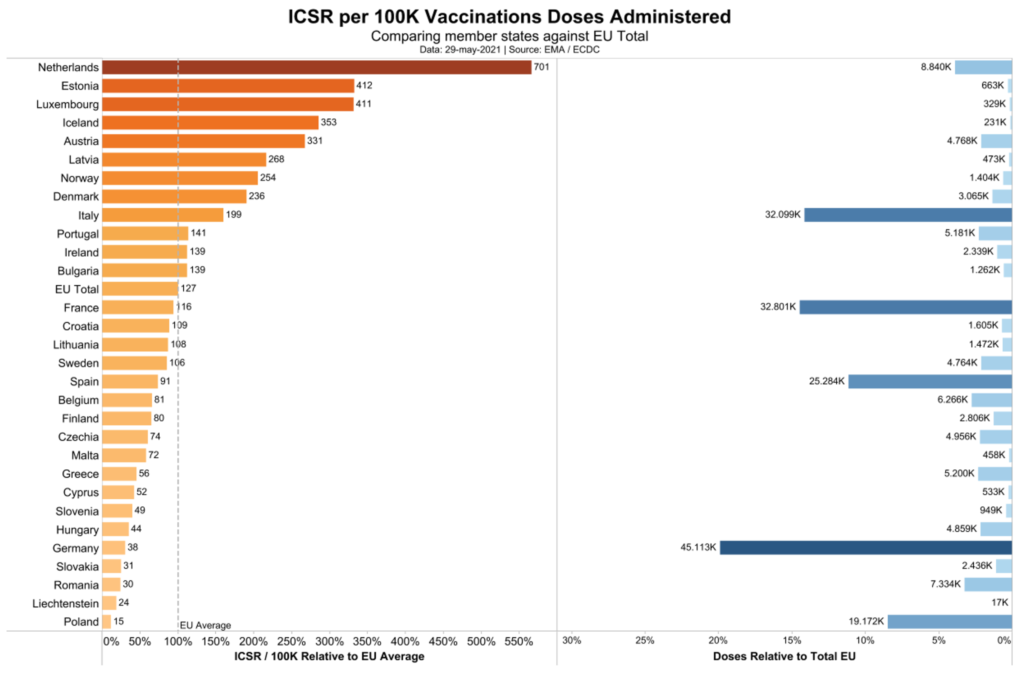
Źródło: https://www.mdpi.com/2076-393X/9/7/693
Poniżej znajduje się spis petycji, które zostały dotychczas odrzucone przez Ministra Zdrowia. Wszystkie te petycje zawierały pomysły pomagające w zwiększeniu skuteczności zgłaszania NOP.
Petycje były składane jeszcze przed „erą kowida” więc dotyczą szczepień obowiązkowych wykonywanych na dzieciach. Gdyby wtedy zostały wdrożone w życie, dziś bylibyśmy już w zupełnie innej rzeczywistości, jeśli chodzi o rzetelność monitorowania NOP po szczepieniu przeciw COVID-19.
-
Minister Zdrowia nie chce wiedzieć, co który NOP jest przez lekarzy zgłaszany – petycja o zbadanie skuteczności systemu zgłaszania NOP została odrzucona.
-
Petycja ws. opublikowania komunikatu dotyczącego rozpoznawania przez lekarzy niepożądanych odczynów poszczepiennych została odrzucona, a więc Minister Zdrowia nie chce nawet przypomnieć lekarzom, czym jest NOP i kiedy należy go zgłosić.
-
Minister Zdrowia nie chce wiedzieć, jak często dochodzi do zgonów wkrótce po szczepieniu i jakie są najczęstsze przyczyny takich zgonów – petycja o gromadzenie danych o zgonach w następstwie czasowym szczepienia została odrzucona.
-
Także petycja o uzupełnienie karty zgonu o rubrykę z datą ostatniego szczepienia została odrzucona. Gdyby zmiany, o które wnosiliśmy, weszły w życie, to dziś Polska mogłaby się pochwalić najdokładniejszą na świecie bazą zgonów po szczepieniu na COVID-19.
-
Pomimo że hospitalizacja do 4 tygodni od szczepienia, to ciężki NOP, to petycja ws. utworzenia normy prawnej zobowiązującej lekarza do ustalenia daty ostatniego szczepienia dziecka chorego poddawanego hospitalizacji także została odrzucona.
-
Minister Zdrowia nie chce nauczyć lekarzy, jak poprawnie wykrywać niepożądane odczyny poszczepienne (petycja o przeprowadzenie wśród lekarzy kampanii informacyjnej dotyczącej prawidłowego rozpoznawania niepożądanych odczynów poszczepiennych została odrzucona).
Zgodnie z art. 13 ust. 2 ustawy o petycjach, sposób załatwienia petycji nie może być przedmiotem skargi więc nie można się w żaden sposób odwołać od odrzucenia petycji.